Nutzen Sie unsere Vorlagen mit hilfreichen Anleitungen zur Erstellung Ihrer technischen Dokumentation oder Ihres QMS. Sparen Sie noch mehr Zeit mit vorausgefüllten, individualisierten Vorlagen mit Ihrem Logo.
Wir prüfen oder erstellen ausgewählte Dokumente oder komplette technische Dokumentationen von Medizin- oder IVD-Produkten. Dabei stellen wir sicher, dass sie MDR- oder IVDR-konform sind.
Richten Sie Ihr QMS ein, indem Sie unsere Vorlagen, unseren Input oder unsere tatkräftige Unterstützung nutzen, oder lassen Sie uns (fast) die ganze Arbeit machen. Welchen Weg Sie auch wählen, wir machen Ihr QMS auditfähig.
Kommen Sie mit Ihren Fragen zu uns. Wir bieten Ihnen Antworten und Lösungen für Themen im Zusammenhang mit Verordnungen, Normen, QMS, strategischen Entscheidungen, CE-Kennzeichnung oder Marktzugang.
Sie möchten eine Leistungsstudie gemäß IVDR durchführen, aber Ihr Unternehmen ist nicht in der Union ansässig? Wir übernehmen die Rolle des rechtlichen Vertreters gerne für Sie. Kontaktieren Sie uns noch heute und erfahren Sie mehr.
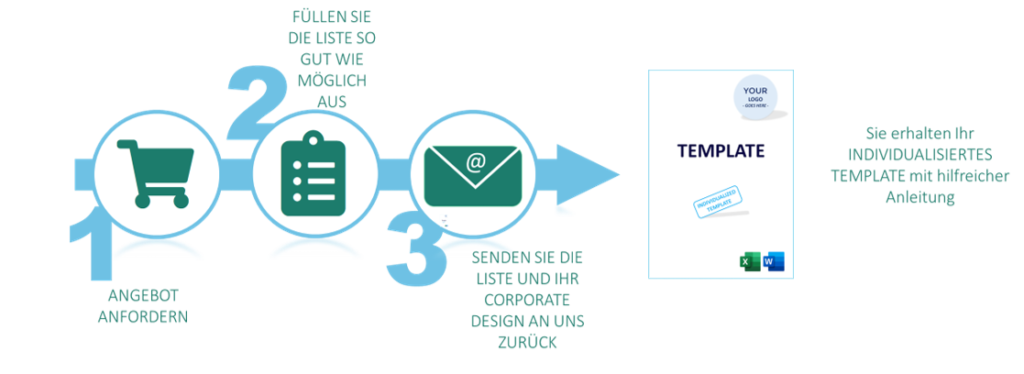
Die Erstellung der technischen Dokumentation für Ihr Medizin- oder IVD-Produkt kann eine komplizierte und zeitaufwändige Angelegenheit sein. Das muss nicht sein: Wir bieten Ihnen Vorlagen mit Hilfestellungen. Darüber hinaus bieten wir individualisierte Vorlagen an. Insgesamt ermöglicht Ihnen diese einzigartige Dienstleistung von AstraCon eine noch schnellere Fertigstellung Ihrer Dokumente.
Ein Schnellcheck für Hersteller, Investoren und Bevollmächtigte Vertreter!
Viele Akteure sind sich unsicher über die Qualität und Vollständigkeit der technischen Dokumentation. Da die technische Dokumentation das regulatorische Herzstück Ihres Medizin- oder IVD-Produkts (MDR/IVDR) ist, müssen Sie über alle Mängel Bescheid wissen. Unsere GAP-Analyse verschafft Ihnen einen umfassenden Überblick. So können Sie sich auf die größten Probleme und Defizite konzentrieren.
Dies ist nicht nur wichtig, wenn Sie ein Hersteller sind und daher über eine eigene technische Dokumentation verfügen. Es kann auch wichtig sein, wenn Sie ein Investor oder ein EU Bevollmächtigter Vertreter sind und unsicher sind, ob die Qualität der Dokumentation Ihres Partnerunternehmens ausreichend ist.
Manchmal reicht jedoch eine schnelle Prüfung für Ihre Zwecke nicht aus. Stattdessen benötigen Sie vielleicht eine detaillierte Prüfung der Einhaltung der MDR oder IVDR. In diesem Fall könnte eine Dokumentenprüfung durch unsere Experten die bessere Option sein. Bei der Überprüfung prüfen unsere Experten, ob alle Anforderungen der MDR/IVDR-Vorschriften, der geltenden harmonisierten Normen sowie der anerkannten Guidance-Dokumente erfüllt sind. So können Sie Ihre Dokumentation schnell und effizient auditfähig machen.
Sie benötigen eine technische Dokumentation für Ihre EU-Markteinführung? Ob einzelne Dokumente oder die gesamte Technische Dokumentation: Unsere Experten arbeiten schnell, zuverlässig und sichern höchste Qualität. In enger Absprache mit Ihnen werden auditfähige Dokumente erstellt.
Ihr QMS ist veraltet, ein Audit steht an, oder Sie sind sich nicht sicher, ob es der ISO 13485 entspricht? Unsere Experten führen eine gründliche Konformitätsprüfung einzelner Dokumente oder Ihres gesamten QMS durch. Unsere Experten überprüfen Ihre Dokumente (insbesondere Ihr QM-Handbuch und die Dokumente der obersten Ebene, wie z. B. Prozessbeschreibungen) und erstellen eine detaillierte Bewertung unter Berücksichtigung der neuesten harmonisierten Normen und Vorschriften. Mit unserer Anleitung sind Ihre Dokumente in kürzester Zeit auditfähig.
Ihr Unternehmen benötigt ein funktionierendes Qualitätsmanagementsystem? Ihnen fehlen jedoch die Zeit und die Ressourcen, um ein eigenes QM-System aufzubauen. Dann lassen Sie sich von unseren Experten bei der Überprüfung oder Erstellung Ihres QM-Systems unterstützen. Ob einzelne Dokumente oder das gesamte QM-System: Unsere Experten arbeiten schnell, zuverlässig und sichern höchste Qualität. Auditfähige Dokumente werden in enger Abstimmung mit Ihnen erstellt.
Sie wollen wissen, ob Ihr QM-System auditfähig ist? In diesem Fall führen wir für Sie ISO 13485-konforme interne Audits in Ihrem Unternehmen oder bei Ihren Lieferanten durch. Unsere qualifizierten Auditoren bereiten alle notwendigen Unterlagen für ein erfolgreiches Audit vor: Auditplan, Auditagenda und natürlich auch den Auditbericht.
Verordnungen wie MDR und IVDR zu verstehen und diese effizient umzusetzen, ist oft kompliziert. Wie ein Bergführer führen unsere Experten Sie auf den Gipfel des Regulierungsbergs, je nach Ihren individuellen Bedürfnissen und Fähigkeiten. Insbesondere werden sie alle Ihre Fragen bestmöglich beantworten und Ihnen dabei helfen, die entspannteste, sicherste, schnellste, kürzeste oder lehrreichste Regulierungsroute zu finden. Sie können sich darauf verlassen, dass unsere Antworten Sie Ihrem Ziel näher bringen – der Zertifizierung nach ISO 13485 oder der CE-Kennzeichnung und EU-Marktzulassung Ihres IVD- oder Medizinprodukts.
Die Auswahl einer Benannten Stelle ist ein wichtiger Schritt auf Ihrem Weg zum CE, insbesondere in Zeiten geringer Audit- und Prüfkapazitäten bei Benannten Stellen. Wir können Sie bei der Auswahl einer geeigneten Benannten Stelle unterstützen – unter Berücksichtigung Ihrer unternehmensweiten Regulierungsstrategie. Darüber hinaus können wir die Kommunikation mit der Benannten Stelle komplett für Sie übernehmen. Selbstverständlich gehört auch die Klärung von Nichtkonformitäten gemeinsam mit Ihnen zu unserem Portfolio.
Sie planen die Durchführung einer Leistungsstudie gemäß IVDR (EU) 2017/746 in einem oder mehreren Ländern der Union? In diesem Fall benötigen Sie einen rechtlichen Vertreter, der für die Einhaltung Ihrer Verpflichtungen gemäß IVDR verantwortlich ist und in Ihrem Namen als Ansprechpartner fungiert (IVDR Artikel 58). AstraCon kann diese Verantwortlichkeiten übernehmen. Bei Bedarf können wir Sie auch bei der Planung und Durchführung Ihrer Einreichungsstrategie unterstützen.
Kontakt aufnehmen
VORLAGEN
TECHNISCHE DOKUMENTATION
MDR / IVDR
ISO 13485
Regulatorische Beratung / Hilfe mit Benannten Stellen
RECHTLICHER VERTRETER
Sie müssen den Inhalt von reCAPTCHA laden, um das Formular abzuschicken. Bitte beachten Sie, dass dabei Daten mit Drittanbietern ausgetauscht werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von Facebook. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von Instagram. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr InformationenSie sehen gerade einen Platzhalterinhalt von X. Um auf den eigentlichen Inhalt zuzugreifen, klicken Sie auf die Schaltfläche unten. Bitte beachten Sie, dass dabei Daten an Drittanbieter weitergegeben werden.
Mehr Informationen